 l l Выяснение структурной организации белков – одна из главных проблем современной биохимии Оно имеет важное научно-практическое значение для понимания огромного разнообразия функций белков Белковые молекулы – продукт поликонденсации 20 -ти различных аминокислот, соединенных не хаотично, а в строгом соответствии с кодом белкового синтеза Каким образом соединяются между собой многие десятки и сотни аминокислот в белковой молекуле?
l l Выяснение структурной организации белков – одна из главных проблем современной биохимии Оно имеет важное научно-практическое значение для понимания огромного разнообразия функций белков Белковые молекулы – продукт поликонденсации 20 -ти различных аминокислот, соединенных не хаотично, а в строгом соответствии с кодом белкового синтеза Каким образом соединяются между собой многие десятки и сотни аминокислот в белковой молекуле?
 Полипептидная теория строения белка l l 1902 г. , Эмиль Фишер Белки – сложные полипептиды, в которых отдельные аминокислоты связаны друг с другом пептидными (R–CO–NH–R) связями, возникающими при взаимодействии карбоксильных и аминогрупп аминокислот
Полипептидная теория строения белка l l 1902 г. , Эмиль Фишер Белки – сложные полипептиды, в которых отдельные аминокислоты связаны друг с другом пептидными (R–CO–NH–R) связями, возникающими при взаимодействии карбоксильных и аминогрупп аминокислот
 Экспериментальные доказательства теории l l l В природных белках сравнительно мало свободных групп –СООН и –NH 2 В процессе гидролиза белка образуется стехиометрическое количество титруемых групп – СООН и –NH 2 Под действием протеолитических ферментов белки расщепляются на строго определенные фрагменты (полипептиды) с концевыми аминокислотами, соответствующими избирательности действия ферментов Белки дают биуретовую реакцию Анализ рентгенограмм подтверждает полипептидную структуру белка Существенное подтверждение полипептидной теории строения белка – возможность синтеза химическими методами полипептидов и белков с уже известным строением (инсулина, лизоцима, рибонуклеазы и др.)
Экспериментальные доказательства теории l l l В природных белках сравнительно мало свободных групп –СООН и –NH 2 В процессе гидролиза белка образуется стехиометрическое количество титруемых групп – СООН и –NH 2 Под действием протеолитических ферментов белки расщепляются на строго определенные фрагменты (полипептиды) с концевыми аминокислотами, соответствующими избирательности действия ферментов Белки дают биуретовую реакцию Анализ рентгенограмм подтверждает полипептидную структуру белка Существенное подтверждение полипептидной теории строения белка – возможность синтеза химическими методами полипептидов и белков с уже известным строением (инсулина, лизоцима, рибонуклеазы и др.)

 Структурные особенности пептидной цепи l l Пептидная связь примерно на 10% короче связи –С–N– и имеет характер «частично двойной» связи –С=N– Л. Полинг и Р. Кори предложили в 1948– 1955 гг. объяснять особую природу связи С–N «резонансом» между двумя формами
Структурные особенности пептидной цепи l l Пептидная связь примерно на 10% короче связи –С–N– и имеет характер «частично двойной» связи –С=N– Л. Полинг и Р. Кори предложили в 1948– 1955 гг. объяснять особую природу связи С–N «резонансом» между двумя формами
 Структурные особенности пептидной цепи l l l Другими словами, в белках и пептидах связь С–N является частично кратной из-за взаимодействия неподеленной пары электронов атома азота с электронной системой карбонильной группы, что приводит к затрудненному вращению вокруг связи С–N Обычно пептидная связь имеет транс-конфигурацию, что выгоднее цис-конфигурации на 2, 6 ккал/моль (10, 878 к. Дж/моль), т. к. сближение -углеродных атомов в цисконфигурации вызывает пространственные затруднения Эта разница в значительной мере снимается, если азот пептидной связи принадлежит про
Структурные особенности пептидной цепи l l l Другими словами, в белках и пептидах связь С–N является частично кратной из-за взаимодействия неподеленной пары электронов атома азота с электронной системой карбонильной группы, что приводит к затрудненному вращению вокруг связи С–N Обычно пептидная связь имеет транс-конфигурацию, что выгоднее цис-конфигурации на 2, 6 ккал/моль (10, 878 к. Дж/моль), т. к. сближение -углеродных атомов в цисконфигурации вызывает пространственные затруднения Эта разница в значительной мере снимается, если азот пептидной связи принадлежит про
 Структурные особенности пептидной цепи l l l Повороты возможны вокруг двух простых связей (N–С и С –C 1), примыкающих к асимметрическому атому Такие повороты измеряются двугранными углами и Любые конформации пептидной цепи могут быть описаны набором значений углов и у каждого из С -атомов (обычно = 180 – транс-форма)
Структурные особенности пептидной цепи l l l Повороты возможны вокруг двух простых связей (N–С и С –C 1), примыкающих к асимметрическому атому Такие повороты измеряются двугранными углами и Любые конформации пептидной цепи могут быть описаны набором значений углов и у каждого из С -атомов (обычно = 180 – транс-форма)
 Структурные особенности пептидной цепи l l В силу взаимодействия между заместителями в пептидной цепи углы и не могут принимать любые значения – для них разрешенными оказываются лишь некоторые дискретные области, соответствующие энергетически выгодным конформациям пептидной цепи Углы и взаимосвязаны, изменение одного из них влечет изменение второго Гопалачамудрам Нарайана Рамачандран
Структурные особенности пептидной цепи l l В силу взаимодействия между заместителями в пептидной цепи углы и не могут принимать любые значения – для них разрешенными оказываются лишь некоторые дискретные области, соответствующие энергетически выгодным конформациям пептидной цепи Углы и взаимосвязаны, изменение одного из них влечет изменение второго Гопалачамудрам Нарайана Рамачандран

 l К. У. Линдерстрем-Ланг предложил различать 4 уровня организации белковых молекул – первичную, вторичную, третичную и четвертичную структуры. Хотя эти категории в известной степени устарели, ими пока продолжают пользоваться
l К. У. Линдерстрем-Ланг предложил различать 4 уровня организации белковых молекул – первичную, вторичную, третичную и четвертичную структуры. Хотя эти категории в известной степени устарели, ими пока продолжают пользоваться

 Первичная структура белка l l l последовательность аминокислотных остатков в полипептидной цепи кодируется структурным геном данного белка и содержит в себе все необходимое для самоорганизации его пространственной структуры Все белки различаются по своей первичной структуре Потенциально возможное число таких структур неограниченно Однако в живой природе все эти возможности не реализуются: общее число различных типов белков у всех видов живых организмов составляет величину порядка 1010– 1012
Первичная структура белка l l l последовательность аминокислотных остатков в полипептидной цепи кодируется структурным геном данного белка и содержит в себе все необходимое для самоорганизации его пространственной структуры Все белки различаются по своей первичной структуре Потенциально возможное число таких структур неограниченно Однако в живой природе все эти возможности не реализуются: общее число различных типов белков у всех видов живых организмов составляет величину порядка 1010– 1012
 l l l Познание биологической функции и, в частности, молекулярного механизма физиологического действия белка невозможно без детального знания его строения Установление первичной структуры белка – основа для определения вторичной и третичной структур, выяснения расположения функциональных групп в его активном центре, путь к познанию механизма его функционирования. Исследование первичной структуры «мутагенных» белков позволяет на молекулярном уровне выяснить характер наследственных болезней Данные по первичной структуре используются как один из показателей при установлении и проверке таксономических взаимоотношений между различными видами живых организмов и построении схемы биологической эволюции
l l l Познание биологической функции и, в частности, молекулярного механизма физиологического действия белка невозможно без детального знания его строения Установление первичной структуры белка – основа для определения вторичной и третичной структур, выяснения расположения функциональных групп в его активном центре, путь к познанию механизма его функционирования. Исследование первичной структуры «мутагенных» белков позволяет на молекулярном уровне выяснить характер наследственных болезней Данные по первичной структуре используются как один из показателей при установлении и проверке таксономических взаимоотношений между различными видами живых организмов и построении схемы биологической эволюции
 Методы определения первичной структуры l l Подготовка белка к анализу первичной структуры призвана свести к минимуму влияние других, более высоких уровней его организации Иными словами, объектом анализа должна быть неупорядоченная белковая цепь без каких-либо поперечных ковалентных связей (например, дисульфидных) так, чтобы все ее звенья, все пептидные связи были в равной мере доступны действию как химических реагентов, так и ферментов
Методы определения первичной структуры l l Подготовка белка к анализу первичной структуры призвана свести к минимуму влияние других, более высоких уровней его организации Иными словами, объектом анализа должна быть неупорядоченная белковая цепь без каких-либо поперечных ковалентных связей (например, дисульфидных) так, чтобы все ее звенья, все пептидные связи были в равной мере доступны действию как химических реагентов, так и ферментов
 l l Белок должен быть прежде всего подвергнут глубокой денатурации и утратить четвертичную, третичную и по возможности вторичную структуры Если в нем имеются дисульфидные связи, прибегают к их расщеплению, используя, как правило, восстановление большим избытком меркаптосоединения
l l Белок должен быть прежде всего подвергнут глубокой денатурации и утратить четвертичную, третичную и по возможности вторичную структуры Если в нем имеются дисульфидные связи, прибегают к их расщеплению, используя, как правило, восстановление большим избытком меркаптосоединения
 l Во избежание замыкания дисульфидных связей вновь сульфгидрильные группы блокируют избытком иодуксусной кислоты: R–SН + I–СН 2–СООН R–S–СН 2–СООН + НI
l Во избежание замыкания дисульфидных связей вновь сульфгидрильные группы блокируют избытком иодуксусной кислоты: R–SН + I–СН 2–СООН R–S–СН 2–СООН + НI
 Затем проводят селективный гидролиз денатурированного белка для получения системы перекрывающихся пептидов. Гидролиз проводят ферментами: l l l трипсином (связи, образованные карбоксильными группами арг или лиз), химотрипсином (связи, образованные группами –СООН ароматических аминокислот) и др. ; химическими реагентами: бромцианом Br –С N (связи, образованные группами –СООН мет) и др.
Затем проводят селективный гидролиз денатурированного белка для получения системы перекрывающихся пептидов. Гидролиз проводят ферментами: l l l трипсином (связи, образованные карбоксильными группами арг или лиз), химотрипсином (связи, образованные группами –СООН ароматических аминокислот) и др. ; химическими реагентами: бромцианом Br –С N (связи, образованные группами –СООН мет) и др.
 l l l Следующий этап – фракционирование полученных пептидов – осуществляется методами хроматографии Наконец, последний этап – определение первичной структуры l начинается с определения его молекулярной массы, аминокислотного состава, N- и Сконцевых аминокислотных остатков После того, как структура всех фрагментов установлена, белок подвергают расщеплению при помощи другого агента и получают второй, отличный от первого набор пептидных фрагментов, которые разделяют и анализируют для выяснения порядка расположения аминокислот в белке
l l l Следующий этап – фракционирование полученных пептидов – осуществляется методами хроматографии Наконец, последний этап – определение первичной структуры l начинается с определения его молекулярной массы, аминокислотного состава, N- и Сконцевых аминокислотных остатков После того, как структура всех фрагментов установлена, белок подвергают расщеплению при помощи другого агента и получают второй, отличный от первого набор пептидных фрагментов, которые разделяют и анализируют для выяснения порядка расположения аминокислот в белке

 Метод Ф. Сенджера l В 1945 г. английский биохимик Ф. Сенджер предложил один из первых методов определения N-концевых аминокислот
Метод Ф. Сенджера l В 1945 г. английский биохимик Ф. Сенджер предложил один из первых методов определения N-концевых аминокислот
 Метод Ф. Сенджера l Раствор белка (пептида) обрабатывают 2, 4 динитрофторбензолом (ДНФ), который со свободной аминогруппой дает динитрофенильное (ДНФ)-производное, окрашенное в желтый цвет:
Метод Ф. Сенджера l Раствор белка (пептида) обрабатывают 2, 4 динитрофторбензолом (ДНФ), который со свободной аминогруппой дает динитрофенильное (ДНФ)-производное, окрашенное в желтый цвет:
 Метод Ф. Сенджера l l Последующий кислотный гидролиз (5, 7 н. НСl) приводит к разрыву пептидных связей и образованию ДНФ-производного Nконцевой аминокислоты Последнее экстрагируется эфиром и идентифицируется методом ТСХ в присутствии стандартов
Метод Ф. Сенджера l l Последующий кислотный гидролиз (5, 7 н. НСl) приводит к разрыву пептидных связей и образованию ДНФ-производного Nконцевой аминокислоты Последнее экстрагируется эфиром и идентифицируется методом ТСХ в присутствии стандартов
 Дансильный метод l Разработан в 1963 г. английскими биохимиками В. Греем и Б. Хартли l Также основан на введении в аминогруппы белка «метки» , не удаляющейся при последующем гидролизе Брайен Хартли
Дансильный метод l Разработан в 1963 г. английскими биохимиками В. Греем и Б. Хартли l Также основан на введении в аминогруппы белка «метки» , не удаляющейся при последующем гидролизе Брайен Хартли
 Дансильный метод l Первая стадия – реакция дансилхлорида (1 -диметиламинонафталин-5 -сульфохлорида) с непротонированной -аминогруппой пептида (или белка) с образованием дансилпептида (ДНС-пептида)
Дансильный метод l Первая стадия – реакция дансилхлорида (1 -диметиламинонафталин-5 -сульфохлорида) с непротонированной -аминогруппой пептида (или белка) с образованием дансилпептида (ДНС-пептида)

 Дансильный метод l Полученный ДНС-белок подвергается гидролизу в присутствии 5, 7 н. НСl, при 105 С в течение 12– 16 ч, отщепившуюся ДНС-аминокислоту идентифицируют по флуоресценции в УФ-лучах
Дансильный метод l Полученный ДНС-белок подвергается гидролизу в присутствии 5, 7 н. НСl, при 105 С в течение 12– 16 ч, отщепившуюся ДНС-аминокислоту идентифицируют по флуоресценции в УФ-лучах


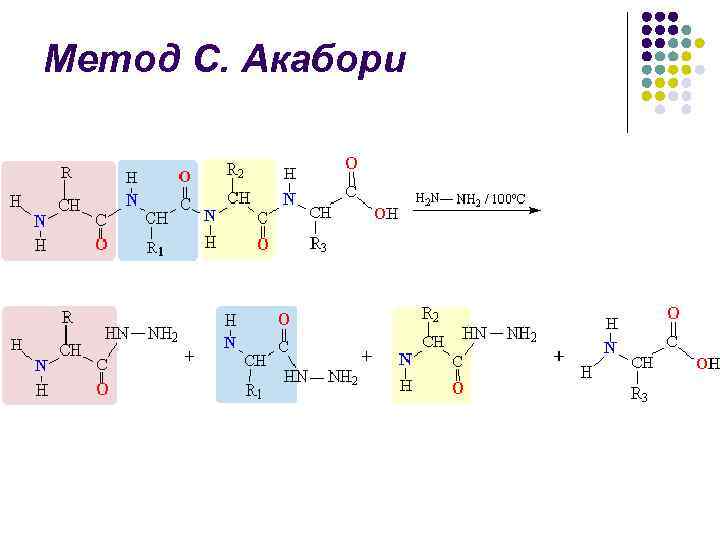 Метод С. Акабори l l При нагревании пептида (или белка) с безводным гидразином при 100– 120 С пептидные связи гидролизуются с образованием гидразидов аминокислот С-концевая аминокислота остается в виде свободной аминокислоты и может быть выделена из смеси и идентифицирована:
Метод С. Акабори l l При нагревании пептида (или белка) с безводным гидразином при 100– 120 С пептидные связи гидролизуются с образованием гидразидов аминокислот С-концевая аминокислота остается в виде свободной аминокислоты и может быть выделена из смеси и идентифицирована:

 Метод П. Эдмана l Метод деградации полипептидной цепи с помощью фенилизотиоционата (ФИТЦ) разработан шведским химиком П. В. Эдманом в 1950– 56 гг. l Метод Эдмана позволяет последовательно отщеплять N-концевые аминокислотные остатки в виде фенилтиогидантоинов (ФТГ) l Каждый цикл деградации включает 3 стадии
Метод П. Эдмана l Метод деградации полипептидной цепи с помощью фенилизотиоционата (ФИТЦ) разработан шведским химиком П. В. Эдманом в 1950– 56 гг. l Метод Эдмана позволяет последовательно отщеплять N-концевые аминокислотные остатки в виде фенилтиогидантоинов (ФТГ) l Каждый цикл деградации включает 3 стадии
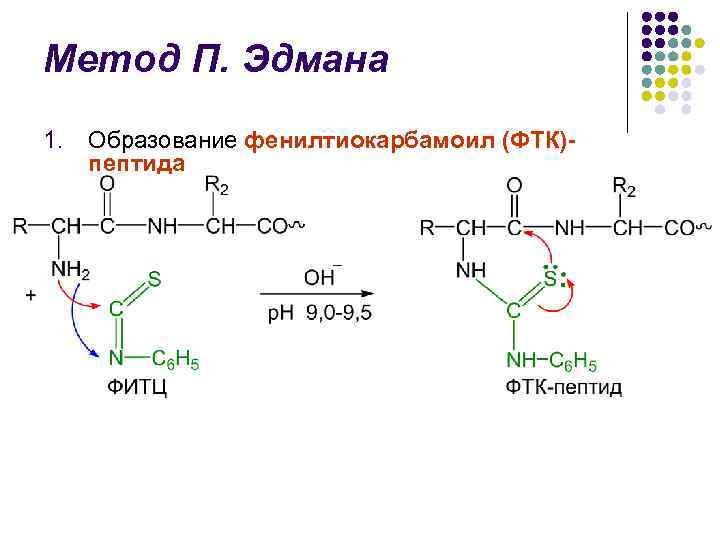

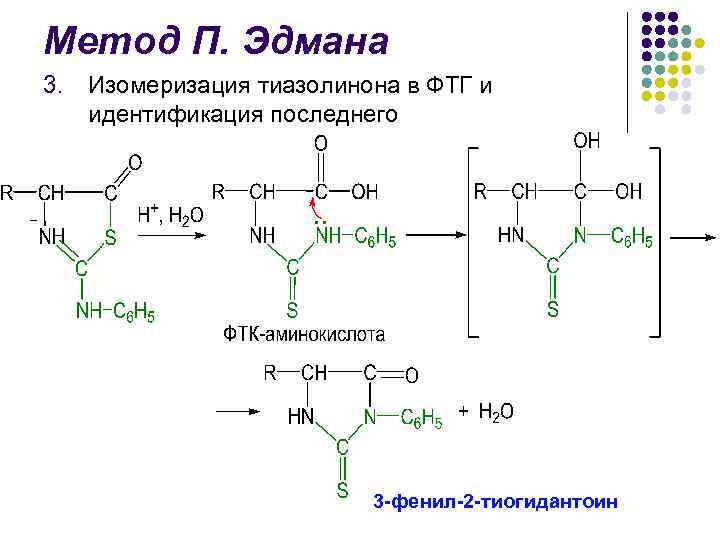

 Метод П. Эдмана l l l Идентификация отщепленных ФТГ является определяющей в методе Эдмана В течение длительного времени использовали хроматографию на бумаге, затем микротонкослойную хроматографию на силикагеле и полиамиде, жидкостную и газо-жидкостную хроматографии Крупным достижением в области структурных исследований белков явилось создание в 1967 г. П. Эдманом и Дж. Бэггом секвенатора (от англ. sequence – последовательность) – прибора, который с высокой эффективностью осуществляет последовательное автоматическое отщепление N-концевых аминокислотных остатков по методу Эдмана
Метод П. Эдмана l l l Идентификация отщепленных ФТГ является определяющей в методе Эдмана В течение длительного времени использовали хроматографию на бумаге, затем микротонкослойную хроматографию на силикагеле и полиамиде, жидкостную и газо-жидкостную хроматографии Крупным достижением в области структурных исследований белков явилось создание в 1967 г. П. Эдманом и Дж. Бэггом секвенатора (от англ. sequence – последовательность) – прибора, который с высокой эффективностью осуществляет последовательное автоматическое отщепление N-концевых аминокислотных остатков по методу Эдмана
 l Для определения структуры пептидов и белков можно применять: l l ферменты, катализирующие отщепление N- и С-концевых аминокислотных остатков – аминои карбоксипептидазы физико-химические методы, в частности, масс-спектрометрию
l Для определения структуры пептидов и белков можно применять: l l ферменты, катализирующие отщепление N- и С-концевых аминокислотных остатков – аминои карбоксипептидазы физико-химические методы, в частности, масс-спектрометрию
 Анализ данных по первичной структуре позволяет сделать следующие общие выводы l l Стабильность первичной структуры обеспечивается в основном пептидными связями; возможно участие и небольшого числа дисульфидных связей В полипептидной цепи могут быть обнаружены разнообразные комбинации аминокислот В полипептидах были открыты все мыслимые дипептиды В полипептидах относительно редки повторяющиеся последовательности
Анализ данных по первичной структуре позволяет сделать следующие общие выводы l l Стабильность первичной структуры обеспечивается в основном пептидными связями; возможно участие и небольшого числа дисульфидных связей В полипептидной цепи могут быть обнаружены разнообразные комбинации аминокислот В полипептидах были открыты все мыслимые дипептиды В полипептидах относительно редки повторяющиеся последовательности
 Анализ данных по первичной структуре позволяет сделать следующие общие выводы l l Каждый индивидуальный гомогенный белок характеризуется уникальной первичной структурой; часто замены аминокислот приводят не только к структурным перестройкам, но и к изменениям физикохимических свойств и биологических функций В некоторых белках (особенно ферментах), обладающих близкими свойствами, встречаются идентичные пептидные структуры (последовательности аминокислот), в особенности в областях их активных центров. Этот принцип структурного подобия наиболее типичен для ряда протеолитических ферментов – трипсина, химотрипсина и др.
Анализ данных по первичной структуре позволяет сделать следующие общие выводы l l Каждый индивидуальный гомогенный белок характеризуется уникальной первичной структурой; часто замены аминокислот приводят не только к структурным перестройкам, но и к изменениям физикохимических свойств и биологических функций В некоторых белках (особенно ферментах), обладающих близкими свойствами, встречаются идентичные пептидные структуры (последовательности аминокислот), в особенности в областях их активных центров. Этот принцип структурного подобия наиболее типичен для ряда протеолитических ферментов – трипсина, химотрипсина и др.

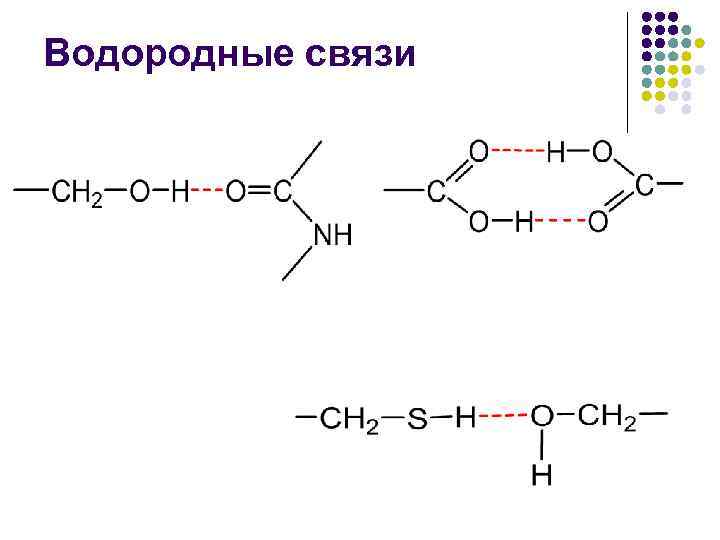
 Водородные связи В неполярном окружении энергия водородной связи –СО НN– составляет около 16, 7 к. Дж/моль, а повышение полярности среды снижает эту энергию
Водородные связи В неполярном окружении энергия водородной связи –СО НN– составляет около 16, 7 к. Дж/моль, а повышение полярности среды снижает эту энергию
 Гидрофобные взаимодействия l l Имеют энтропийную природу Связаны с тем, что неполярные заместители выталкиваются из воды и стремятся ограничить свой контакт с ней Напротив, вода стремится восстановить свое структурированное состояние и как бы принудительно группирует заместители в кластеры, обладающие минимумом энергии Вступают в основном неполярные боковые группы аминокислотных остатков
Гидрофобные взаимодействия l l Имеют энтропийную природу Связаны с тем, что неполярные заместители выталкиваются из воды и стремятся ограничить свой контакт с ней Напротив, вода стремится восстановить свое структурированное состояние и как бы принудительно группирует заместители в кластеры, обладающие минимумом энергии Вступают в основном неполярные боковые группы аминокислотных остатков

 Ван-дер-ваальсовы взаимодействия l l Складываются из дисперсионных сил притяжения атомов и сил взаимного отталкивания их электронных оболочек Энергетический вклад каждого контакта невелик (
Ван-дер-ваальсовы взаимодействия l l Складываются из дисперсионных сил притяжения атомов и сил взаимного отталкивания их электронных оболочек Энергетический вклад каждого контакта невелик (
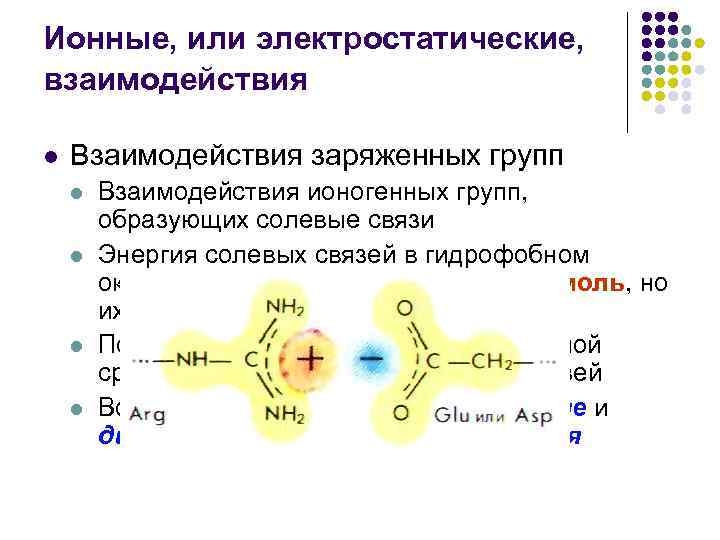 Ионные, или электростатические, взаимодействия l Взаимодействия заряженных групп l l Взаимодействия ионогенных групп, образующих солевые связи Энергия солевых связей в гидрофобном окружении может достигать 41, 9 к. Дж/моль, но их число сравнительно невелико Повышение диэлектрической постоянной среды понижает энергию солевых связей Во многом аналогичны ион-дипольные и диполь-дипольные взаимодействия
Ионные, или электростатические, взаимодействия l Взаимодействия заряженных групп l l Взаимодействия ионогенных групп, образующих солевые связи Энергия солевых связей в гидрофобном окружении может достигать 41, 9 к. Дж/моль, но их число сравнительно невелико Повышение диэлектрической постоянной среды понижает энергию солевых связей Во многом аналогичны ион-дипольные и диполь-дипольные взаимодействия
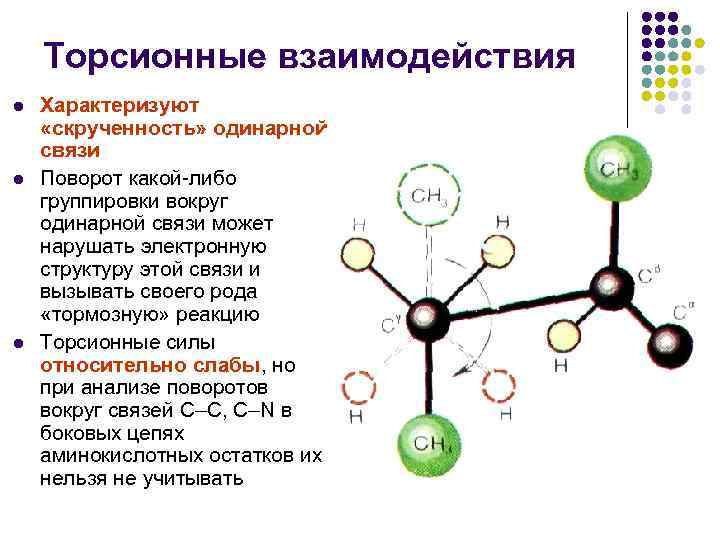 Торсионные взаимодействия l l l Характеризуют «скрученность» одинарной связи Поворот какой-либо группировки вокруг одинарной связи может нарушать электронную структуру этой связи и вызывать своего рода «тормозную» реакцию Торсионные силы относительно слабы, но при анализе поворотов вокруг связей С–С, С–N в боковых цепях аминокислотных остатков их нельзя не учитывать
Торсионные взаимодействия l l l Характеризуют «скрученность» одинарной связи Поворот какой-либо группировки вокруг одинарной связи может нарушать электронную структуру этой связи и вызывать своего рода «тормозную» реакцию Торсионные силы относительно слабы, но при анализе поворотов вокруг связей С–С, С–N в боковых цепях аминокислотных остатков их нельзя не учитывать

 Вторичная структура белка… l l пространственное расположение отдельных участков полипептидной цепи без учета типа и конформации боковых радикалов аминокислот Образуется за счет водородных связей между пептидными группами как одной цепи, так и разных цепей
Вторичная структура белка… l l пространственное расположение отдельных участков полипептидной цепи без учета типа и конформации боковых радикалов аминокислот Образуется за счет водородных связей между пептидными группами как одной цепи, так и разных цепей
 Вторичная структура белка l l l Любой участок молекулы белка имеет вторичную структуру Иногда рассматривают как вторичную структуру только периодические ее элементы: -спираль и -структуру Однако в белках встречаются участки, которые уложены вполне определенным способом, хотя их пространственная структура не содержит какого-либо периодически повторяющегося, регулярного мотива. Тем не менее к ним вполне приложимо понятие вторичной структуры Различают 2 вида вторичных структур: регулярные и нерегулярные Понятие вторичной структуры относится не ко всей белковой молекуле в целом, а к отдельным более или менее протяженным участкам ее полипептидной цепи
Вторичная структура белка l l l Любой участок молекулы белка имеет вторичную структуру Иногда рассматривают как вторичную структуру только периодические ее элементы: -спираль и -структуру Однако в белках встречаются участки, которые уложены вполне определенным способом, хотя их пространственная структура не содержит какого-либо периодически повторяющегося, регулярного мотива. Тем не менее к ним вполне приложимо понятие вторичной структуры Различают 2 вида вторичных структур: регулярные и нерегулярные Понятие вторичной структуры относится не ко всей белковой молекуле в целом, а к отдельным более или менее протяженным участкам ее полипептидной цепи
 Вторичная структура белка l Взаимодействия, которым принадлежит важнейшая роль в формировании вторичной структуры, определяются: l l l особенностями пептидной связи стерическими ограничениями (- и -углы) Основную роль играют водородные связи между периодически повторяющимися в цепи пептидными группировками
Вторичная структура белка l Взаимодействия, которым принадлежит важнейшая роль в формировании вторичной структуры, определяются: l l l особенностями пептидной связи стерическими ограничениями (- и -углы) Основную роль играют водородные связи между периодически повторяющимися в цепи пептидными группировками
 Стабилизация вторичной структуры за счет водородной связи l l Влияние окружающей белок воды Вода способна эффективно конкурировать за образование водородных связей: Влияние воды снижается при формировании компактной пространственной структуры белка, росте содержания пептидных связей, повышении вероятности их взаимодействия Таким образом, стабильность вторичной структуры зависит от ее включения в компактную третичную структуру
Стабилизация вторичной структуры за счет водородной связи l l Влияние окружающей белок воды Вода способна эффективно конкурировать за образование водородных связей: Влияние воды снижается при формировании компактной пространственной структуры белка, росте содержания пептидных связей, повышении вероятности их взаимодействия Таким образом, стабильность вторичной структуры зависит от ее включения в компактную третичную структуру

 -Спираль l В 50 -х годах ХХ в. Л. Полинг и Р. Кори, основываясь на данных о структуре кристаллов аминокислот и простых пептидов, рассмотрели возможные периодические конформации полипептидной цепи и пришли к выводу, что наиболее вероятна структура, названная ими -спиралью
-Спираль l В 50 -х годах ХХ в. Л. Полинг и Р. Кори, основываясь на данных о структуре кристаллов аминокислот и простых пептидов, рассмотрели возможные периодические конформации полипептидной цепи и пришли к выводу, что наиболее вероятна структура, названная ими -спиралью
 -Спираль В основу ее выбора были положены следующие критерии: 1. Образование плотноупакованной компактной структуры без пустот и перекрывания атомов 2. Максимальная насыщенность структуры водородными связями с тем условием, чтобы их геометрия была близка к линейной 3. Соблюдение межатомных расстояний и углов, свойственных аминокислотам и простым пептидам l
-Спираль В основу ее выбора были положены следующие критерии: 1. Образование плотноупакованной компактной структуры без пустот и перекрывания атомов 2. Максимальная насыщенность структуры водородными связями с тем условием, чтобы их геометрия была близка к линейной 3. Соблюдение межатомных расстояний и углов, свойственных аминокислотам и простым пептидам l
 -Спираль l С соблюдением этих условий можно построить как правую, так и левую спирали, однако правая -спираль оказывается энергетически несколько выгоднее левой, если пептидная цепь образована L-аминокислотами
-Спираль l С соблюдением этих условий можно построить как правую, так и левую спирали, однако правая -спираль оказывается энергетически несколько выгоднее левой, если пептидная цепь образована L-аминокислотами
 -Спираль l l Спиральная структура возникает, когда во всех звеньях полипептидной цепи углы поворота вокруг простых связей (и) имеют одинаковую величину и знак (близки к 60), что и приводит к постепенному закручиванию цепи При этом радикалы аминокислотных остатков оказываются на периферии образованного спиралью цилиндра и могут, в зависимости от характера их, обеспечивать гидрофобную или гидрофильную природу цилиндрической поверхности
-Спираль l l Спиральная структура возникает, когда во всех звеньях полипептидной цепи углы поворота вокруг простых связей (и) имеют одинаковую величину и знак (близки к 60), что и приводит к постепенному закручиванию цепи При этом радикалы аминокислотных остатков оказываются на периферии образованного спиралью цилиндра и могут, в зависимости от характера их, обеспечивать гидрофобную или гидрофильную природу цилиндрической поверхности

 -Спираль геометрические параметры: l l l l радиус r = 2, 3 Å (0, 23 нм) высота спирали (смещение) на 1 остаток d = 1, 5 Å шаг спирали (период идентичности) Р = 5, 4 Å 1 виток спирали образуют 3, 6 аминокислотных остатка все связи –С=О ориентированы вперед, к С-концу, а группы –N–Н – назад В -спирали каждая –NНгруппа соединена водородной связью с группой –СО четвертого от нее аминокислотного остатка (5 1 связь)
-Спираль геометрические параметры: l l l l радиус r = 2, 3 Å (0, 23 нм) высота спирали (смещение) на 1 остаток d = 1, 5 Å шаг спирали (период идентичности) Р = 5, 4 Å 1 виток спирали образуют 3, 6 аминокислотных остатка все связи –С=О ориентированы вперед, к С-концу, а группы –N–Н – назад В -спирали каждая –NНгруппа соединена водородной связью с группой –СО четвертого от нее аминокислотного остатка (5 1 связь)
 -Спираль l l Длина -спиральных участков в глобулярных белках относительно невелика (5– 15 аминокислотных остатков, 3 – 4 витка спирали), в фибриллярных белках – гораздо протяженнее Иногда наблюдаются изломы -спирали, обычно в местах включения остатков про, прерывающих системы водородных связей. При этом ось спирали отклоняется на 20– 30
-Спираль l l Длина -спиральных участков в глобулярных белках относительно невелика (5– 15 аминокислотных остатков, 3 – 4 витка спирали), в фибриллярных белках – гораздо протяженнее Иногда наблюдаются изломы -спирали, обычно в местах включения остатков про, прерывающих системы водородных связей. При этом ось спирали отклоняется на 20– 30

 -Структура l l Предложена У. Т. Астбери в 1941 г. на основании рентгеноструктурных исследований -кератина Через 10 лет Л. Полинг и Р. Кори установили, что структура, или «складчатый лист» , – это стабилизированный межцепочечными водородными связями ассоциат вытянутых, зигзагообразных пептидных цепей
-Структура l l Предложена У. Т. Астбери в 1941 г. на основании рентгеноструктурных исследований -кератина Через 10 лет Л. Полинг и Р. Кори установили, что структура, или «складчатый лист» , – это стабилизированный межцепочечными водородными связями ассоциат вытянутых, зигзагообразных пептидных цепей




 -Структура l l Число аминокислотных остатков в отрезке пептидной цепи, образующем -структуру, обычно от 3 до 8 Протяженная -структура, так называемый -слой, или -складчатый лист чаще всего состоит из 2– 6 цепей, иногда до 10
-Структура l l Число аминокислотных остатков в отрезке пептидной цепи, образующем -структуру, обычно от 3 до 8 Протяженная -структура, так называемый -слой, или -складчатый лист чаще всего состоит из 2– 6 цепей, иногда до 10
 -Структура l l l Боковые группы аминокислотных остатков при образовании структуры оказываются по разные стороны ее поверхности Сама же поверхность имеет складчатую форму, причем складки заданы -углеродными атомами Отходящие от них боковые группы образуют гребни Это позволяет формировать довольно протяженные поверхности, насыщенные однотипными (например, гидрофобными) боковыми радикалами Гидрофобные поверхности -складчатого слоя, взаимодействуя между собой или с гидрофобными гребнями -спиралей, участвуют в построении внутримолекулярных гидрофобных ядер, стабилизирующих пространственную структуру белка
-Структура l l l Боковые группы аминокислотных остатков при образовании структуры оказываются по разные стороны ее поверхности Сама же поверхность имеет складчатую форму, причем складки заданы -углеродными атомами Отходящие от них боковые группы образуют гребни Это позволяет формировать довольно протяженные поверхности, насыщенные однотипными (например, гидрофобными) боковыми радикалами Гидрофобные поверхности -складчатого слоя, взаимодействуя между собой или с гидрофобными гребнями -спиралей, участвуют в построении внутримолекулярных гидрофобных ядер, стабилизирующих пространственную структуру белка

 -Изгиб l l Как -спираль, так и -структура обычно представлены в глобулярных белках сравнительно короткими отрезками, поэтому значительная часть вторичной структуры белка приходится на разного рода петли, позволяющие изменить направление пептидной цепи Наиболее экономный структурный элемент, позволяющий повернуть полипептид на 180 , используя всего 3 пептидные группировки, – -изгиб Стабилизируется одной водородной связью Практически всегда оказывается на поверхности белковой глобулы, поэтому нередко играет существенную роль в ее взаимодействии с другими молекулами
-Изгиб l l Как -спираль, так и -структура обычно представлены в глобулярных белках сравнительно короткими отрезками, поэтому значительная часть вторичной структуры белка приходится на разного рода петли, позволяющие изменить направление пептидной цепи Наиболее экономный структурный элемент, позволяющий повернуть полипептид на 180 , используя всего 3 пептидные группировки, – -изгиб Стабилизируется одной водородной связью Практически всегда оказывается на поверхности белковой глобулы, поэтому нередко играет существенную роль в ее взаимодействии с другими молекулами


 l По результатам рентгеноструктурного анализа обнаружено, что способ укладки молекулы белка определяется его аминокислотной последовательностью l l l образованию -спирали способствуют ала, лей, глу образованию -структуры – мет, вал, иле изгибу цепи – гли, про, асн Если из 6 сгруппированных остатков аминокислот 4 способствуют образованию спирали, то данная группа – центр спирализации Если 3 остатка из 5 сгруппированных способствуют образованию -структуры, то данная группировка – затравка для -слоя
l По результатам рентгеноструктурного анализа обнаружено, что способ укладки молекулы белка определяется его аминокислотной последовательностью l l l образованию -спирали способствуют ала, лей, глу образованию -структуры – мет, вал, иле изгибу цепи – гли, про, асн Если из 6 сгруппированных остатков аминокислот 4 способствуют образованию спирали, то данная группа – центр спирализации Если 3 остатка из 5 сгруппированных способствуют образованию -структуры, то данная группировка – затравка для -слоя

 Сверхвторичная (надвторичная) структура белков l l Этот уровень организации белковой молекулы связан с наличием ансамблей взаимодействующих между собой вторичных структур Пространственное строение таких ансамблей и называют сверхвторичной структурой белковой молекулы, которая энергетически наиболее предпочтительна
Сверхвторичная (надвторичная) структура белков l l Этот уровень организации белковой молекулы связан с наличием ансамблей взаимодействующих между собой вторичных структур Пространственное строение таких ансамблей и называют сверхвторичной структурой белковой молекулы, которая энергетически наиболее предпочтительна

 Суперспирализованная -спираль l l Образуется при скручивании нескольких -спиралей в протофибриллы (-кератин), которые объединяются в микрофибриллы -Спирали удерживаются силами Ван-дер-Ваальса
Суперспирализованная -спираль l l Образуется при скручивании нескольких -спиралей в протофибриллы (-кератин), которые объединяются в микрофибриллы -Спирали удерживаются силами Ван-дер-Ваальса

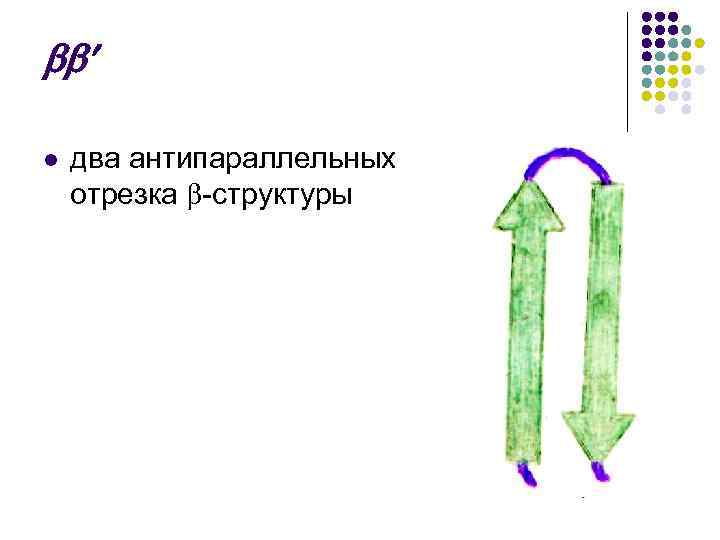
 х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l неупорядоченного клубка – с
х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l неупорядоченного клубка – с
 х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l l -спирали – – укладка цепи по Россману Два последовательно соединенных участка образуют структуру «греческий орнамент» –
х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l l -спирали – – укладка цепи по Россману Два последовательно соединенных участка образуют структуру «греческий орнамент» –
 х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l -структуры – – -зигзаг, «греческий ключ»
х l звено, состоящее из двух параллельных -слоев с сочленением между ними в виде: l -структуры – – -зигзаг, «греческий ключ»

 Домены l l Многие белки содержат относительно слабо взаимодействующие между собой участки – домены Домены (от фр. domaine – владение) – структурно и функционально обособленные области (субобласти) молекулы, соединенные друг с другом короткими участками полипептидной цепи, которые называются шарнирными участками Функциональные домены могут состоять из одного или нескольких структурных доменов У ряда ферментов в углублениях между доменами располагается активный центр
Домены l l Многие белки содержат относительно слабо взаимодействующие между собой участки – домены Домены (от фр. domaine – владение) – структурно и функционально обособленные области (субобласти) молекулы, соединенные друг с другом короткими участками полипептидной цепи, которые называются шарнирными участками Функциональные домены могут состоять из одного или нескольких структурных доменов У ряда ферментов в углублениях между доменами располагается активный центр



 3. + -Белки l имеются участки, целиком построенные из -спиралей, и участки, целиком построенные из антипараллельных -слоев Инсулин
3. + -Белки l имеются участки, целиком построенные из -спиралей, и участки, целиком построенные из антипараллельных -слоев Инсулин

 4. / -Белки l l -Спирали и -структуры чередуются по ходу цепи Большинство -структур (параллельные) оказываются локализованными в центральной части молекулы, где эти структуры изгибаются в виде пропеллера («твист» структуры), образуя жесткую «основу» , с которой связаны остальные участки молекулы
4. / -Белки l l -Спирали и -структуры чередуются по ходу цепи Большинство -структур (параллельные) оказываются локализованными в центральной части молекулы, где эти структуры изгибаются в виде пропеллера («твист» структуры), образуя жесткую «основу» , с которой связаны остальные участки молекулы


 Домены l l l Средний размер домена обычно – 100– 150 остатков, что отвечает глобуле с поперечником около 2, 5 нм Вместе с тем встречаются и значительно большие домены Вероятнее всего, формирование пространственной структуры белка вначале происходит внутри будущих доменов, а взаимная укладка доменов, т. е. образование третичной структуры, происходит на заключительных этапах формирования глобулы
Домены l l l Средний размер домена обычно – 100– 150 остатков, что отвечает глобуле с поперечником около 2, 5 нм Вместе с тем встречаются и значительно большие домены Вероятнее всего, формирование пространственной структуры белка вначале происходит внутри будущих доменов, а взаимная укладка доменов, т. е. образование третичной структуры, происходит на заключительных этапах формирования глобулы

 Третичная структура белка… l l l характеризует пространственное расположение упорядоченных и аморфных участков в полипептидной цепи в целом, которое достигается за счет взаимодействия боковых радикалов и зависит от их типа и конформации Таким образом, третичная структура описывает пространственную укладку всей молекулы белка, если она образована одной полипептидной цепью Имеет прямое отношение к форме молекул белка, которая может быть различной: от шарообразной до нитевидной
Третичная структура белка… l l l характеризует пространственное расположение упорядоченных и аморфных участков в полипептидной цепи в целом, которое достигается за счет взаимодействия боковых радикалов и зависит от их типа и конформации Таким образом, третичная структура описывает пространственную укладку всей молекулы белка, если она образована одной полипептидной цепью Имеет прямое отношение к форме молекул белка, которая может быть различной: от шарообразной до нитевидной
 Нитевидные, или фибриллярные белки l l фиброин шелка кератин волос, рогов, копыт коллаген и др.
Нитевидные, или фибриллярные белки l l фиброин шелка кератин волос, рогов, копыт коллаген и др.

 Третичная структура белка l l основа функциональности белка, которая требует точной пространственной организации больших ансамблей, построенных из множества аминокислотных остатков Такие ансамбли (домены) формируют: l l активные центры ферментов зоны связывания других биологических молекул эффекторные центры белков и т. д. , поэтому нарушение третичной структуры белка (денатурация) неизменно приводит к утрате им способности функционировать
Третичная структура белка l l основа функциональности белка, которая требует точной пространственной организации больших ансамблей, построенных из множества аминокислотных остатков Такие ансамбли (домены) формируют: l l активные центры ферментов зоны связывания других биологических молекул эффекторные центры белков и т. д. , поэтому нарушение третичной структуры белка (денатурация) неизменно приводит к утрате им способности функционировать
 Третичная структура белка l l l Стабильность третичной структуры зависит от системы нековалентных взаимодействий внутри белковой глобулы (?) Некоторые белки дополнительно стабилизируются ковалентными – дисульфидными – связями Gцепь = RТln. К = Нцепь – Т Sцепь Нцепь 0 (S
Третичная структура белка l l l Стабильность третичной структуры зависит от системы нековалентных взаимодействий внутри белковой глобулы (?) Некоторые белки дополнительно стабилизируются ковалентными – дисульфидными – связями Gцепь = RТln. К = Нцепь – Т Sцепь Нцепь 0 (S
 Третичная структура белка l Соотношение Нцепь и –Т Sцепь зависит от: l l числа нековалентных связей, устанавливающихся при свертывании молекулы белка в глобулу, а значит, от длины полипептидной цепи от температуры. С ростом Т |Т S| рано или поздно превысит | Н| и пространственная структура утратит стабильность – тепловая денатурация белка
Третичная структура белка l Соотношение Нцепь и –Т Sцепь зависит от: l l числа нековалентных связей, устанавливающихся при свертывании молекулы белка в глобулу, а значит, от длины полипептидной цепи от температуры. С ростом Т |Т S| рано или поздно превысит | Н| и пространственная структура утратит стабильность – тепловая денатурация белка
 Третичная структура белка l l При свертывании глобулы убывает энтропия пептидной цепи, но одновременно происходит возрастание энтропии растворителя – воды Это играет решающую роль в стабилизации третичной структуры
Третичная структура белка l l При свертывании глобулы убывает энтропия пептидной цепи, но одновременно происходит возрастание энтропии растворителя – воды Это играет решающую роль в стабилизации третичной структуры
 Третичная структура белка l l Вода – необычный, в высокой мере структурированный растворитель (?) Полярные группы белка легко включаются в льдоподобные структуры воды, устанавливая с ней водородные связи Неполярные группы занимают своеобразные полости, образованные молекулами воды, связанными водородными связями Все это выключает из хаотического движения значительное число молекул воды, т. е. происходит упорядочение, уменьшение энтропии воды
Третичная структура белка l l Вода – необычный, в высокой мере структурированный растворитель (?) Полярные группы белка легко включаются в льдоподобные структуры воды, устанавливая с ней водородные связи Неполярные группы занимают своеобразные полости, образованные молекулами воды, связанными водородными связями Все это выключает из хаотического движения значительное число молекул воды, т. е. происходит упорядочение, уменьшение энтропии воды
 Третичная структура белка l l l Но так как неполярные группы белка не могут «отслаиваться» от молекулы, происходит свертывание глобулы, при котором значительная часть (не менее ½) гидрофобных групп оказывается скрытой от контакта с водой Это влечет установление гидрофобных контактов, ван-дер-ваальсовых сил Происходит понижение энтропии белка Следствием образования глобулы является разрушение значительной части водородных связей и гидрофобных взаимодействий боковых групп с молекулами воды Возрастает хаотичность движения последних, и энтропия воды растет
Третичная структура белка l l l Но так как неполярные группы белка не могут «отслаиваться» от молекулы, происходит свертывание глобулы, при котором значительная часть (не менее ½) гидрофобных групп оказывается скрытой от контакта с водой Это влечет установление гидрофобных контактов, ван-дер-ваальсовых сил Происходит понижение энтропии белка Следствием образования глобулы является разрушение значительной части водородных связей и гидрофобных взаимодействий боковых групп с молекулами воды Возрастает хаотичность движения последних, и энтропия воды растет

 Четвертичная структура белка… l l l Четвертичную структуру имеют олигомерные белки, молекулы которых состоят из двух и более полипептидных цепей, связанных нековалентно Четвертичная структура – размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями белка Взаимодействие между субъединицами достаточно сильно, так что их ансамбль (ансамбль глобул) выступает как единая молекула, в то же время каждая из объединившихся глобул сохраняет значительную автономность
Четвертичная структура белка… l l l Четвертичную структуру имеют олигомерные белки, молекулы которых состоят из двух и более полипептидных цепей, связанных нековалентно Четвертичная структура – размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями белка Взаимодействие между субъединицами достаточно сильно, так что их ансамбль (ансамбль глобул) выступает как единая молекула, в то же время каждая из объединившихся глобул сохраняет значительную автономность

 Четвертичная структура белка l l Субъединицы, образующие четвертичную структуру белка, могут быть совершенно различными по строению и функциям – гетеромерные белки Это позволяет объединить в одной структуре несколько взаимосвязанных функций, создать полифункциональную молекулу l l Пример. Протеинкиназа: С-субъединица отвечает за ферментативную активность, а R-субъединица – регуляторная В гомомерных белках субъединицы одинаковы
Четвертичная структура белка l l Субъединицы, образующие четвертичную структуру белка, могут быть совершенно различными по строению и функциям – гетеромерные белки Это позволяет объединить в одной структуре несколько взаимосвязанных функций, создать полифункциональную молекулу l l Пример. Протеинкиназа: С-субъединица отвечает за ферментативную активность, а R-субъединица – регуляторная В гомомерных белках субъединицы одинаковы
 Четвертичная структура белка l Межсубъединичные контакты – весьма развитая система нековалентных взаимодействий l l Контакты между гидрофобными группами и целыми гидрофобными участками на поверхности субъединиц (контактные площадки, или зоны), приводящие к возрастанию энтропии системы и сдвигу равновесия в сторону олигомера водородные связи электростатические взаимодействия между боковыми группами Четвертичная структура менее прочная, чем третичная, т. к. меньше вклад гидрофобных контактов
Четвертичная структура белка l Межсубъединичные контакты – весьма развитая система нековалентных взаимодействий l l Контакты между гидрофобными группами и целыми гидрофобными участками на поверхности субъединиц (контактные площадки, или зоны), приводящие к возрастанию энтропии системы и сдвигу равновесия в сторону олигомера водородные связи электростатические взаимодействия между боковыми группами Четвертичная структура менее прочная, чем третичная, т. к. меньше вклад гидрофобных контактов

 Функции четвертичной структуры 1. Объединение нескольких взаимосвязанных функций в единой структуре 2. Архитектурная функция 1. Формирование пространственных образований весьма сложной конфигурации, обеспечивающих специфические функциональные возможности белка (ферритин) 2. Суммарное проведение последовательных реакций ферментами 3. Формирование функциональных центров (активных центров ферментов)
Функции четвертичной структуры 1. Объединение нескольких взаимосвязанных функций в единой структуре 2. Архитектурная функция 1. Формирование пространственных образований весьма сложной конфигурации, обеспечивающих специфические функциональные возможности белка (ферритин) 2. Суммарное проведение последовательных реакций ферментами 3. Формирование функциональных центров (активных центров ферментов)
 Функции четвертичной структуры 3. Обеспечение множественных взаимодействий белка с протяженными структурами l ДНК-связывающие белки – димеры (?) 4. Регуляторная функция. Передача эффекта (нарушение третичной структуры при взаимодействии с субстратом) передается от одной субъединицы к другой, что приводит к перестройке всей четвертичной структуры
Функции четвертичной структуры 3. Обеспечение множественных взаимодействий белка с протяженными структурами l ДНК-связывающие белки – димеры (?) 4. Регуляторная функция. Передача эффекта (нарушение третичной структуры при взаимодействии с субстратом) передается от одной субъединицы к другой, что приводит к перестройке всей четвертичной структуры


 1. Каждый индивидуальный белок характеризуется уникальной структурой, обеспечивающей уникальность его функций 2. Поэтому выяснение структуры разнообразных белков может служить ключом к познанию природы живых систем и, соответственно, сущности жизни
1. Каждый индивидуальный белок характеризуется уникальной структурой, обеспечивающей уникальность его функций 2. Поэтому выяснение структуры разнообразных белков может служить ключом к познанию природы живых систем и, соответственно, сущности жизни
 Литература l l l l Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. – М. : Медицина, 1983 Мецлер Д. Биохимия. Химические реакции в живой клетке. В 3 -х т. – Т. т. 1, 2. – М. : Мир, 1980 Овчинников Ю. А. Биоорганическая химия. – М. : Просвещение, 1987 Основы биохимии / Под ред. А. А. Анисимова. – М. : Высшая школа, 1986 Рис Э. , Стренберг М. От клеток к атомам. Иллюстрированное введение в молекулярную биологию. – М. : Мир, 1988 Степанов В. М. Молекулярная биология. Структура и функции белков. – М. : Высшая школа, 1996 Филиппович Ю. Б. Основы биохимии. – М. : Высшая школа, 1993
Литература l l l l Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. – М. : Медицина, 1983 Мецлер Д. Биохимия. Химические реакции в живой клетке. В 3 -х т. – Т. т. 1, 2. – М. : Мир, 1980 Овчинников Ю. А. Биоорганическая химия. – М. : Просвещение, 1987 Основы биохимии / Под ред. А. А. Анисимова. – М. : Высшая школа, 1986 Рис Э. , Стренберг М. От клеток к атомам. Иллюстрированное введение в молекулярную биологию. – М. : Мир, 1988 Степанов В. М. Молекулярная биология. Структура и функции белков. – М. : Высшая школа, 1996 Филиппович Ю. Б. Основы биохимии. – М. : Высшая школа, 1993
1) группой генов 2) одним геном
3) одной молекулой ДНК 4) совокупностью генов организма
2. Один триплет ДНК несет информацию о:
1) последовательности аминокислот в молекуле белка
2) признаке организма 3) аминокислоте в молекуле синтезируемого белка
4) составе молекулы РНК
3. Теорию матричного синтеза предложил:
1) Дж. Уотсон 3) Г. Де Фриз 2) Н. Кольцов 4) Т. Морган
4. Ген кодирует информацию о последовательности мономеров в молекуле:
1) т-РНК 3) белка 2) гликогена 4) ДНК
5. Какой из процессов происходит в клетках любого строения и функции:
1) синтез белков 3) обмен веществ 2) митоз 4) мейоз
6. Антикодонами называются триплеты:
1) ДНК 3) т-РНК 2) и-РНК 4) р-РНК
7. Понятие «транскрипция» относится к процессу:
1) удвоения ДНК 2) синтеза и-РНК на ДНК
3) перехода и-РНК на рибосомы 4) создания белковых молекул на полисоме
8. Пластический обмен состоит преимущественно из реакций:
1) распада органических веществ 2) распада неорганических веществ
3) синтеза органических веществ 4) синтеза неорганических веществ
9. Участок молекулы ДНК, несущий информацию об одной молекуле бела - это: 1) ген 2) фенотип 3) геном 4) генотип
10. Синтез белка в прокариотической клетке происходит:
1) на рибосомах в ядре 2) на рибосомах в цитоплазме 3) в клеточной стенке
4) на внешней поверхности цитоплазматической мембраны
11. Транскрипция у эукариот происходит в:
1) цитоплазме 2) эндоплазматическом ретикулуме 3) лизосомах 4) ядре
12. Синтез белка происходит в:
1) гранулярном эндоплазматическом ретикулуме
2) гладком эндоплазматическом ретикулуме 3) ядре 4) лизосомах
13. Процесс трансляции не происходит:
1) в цитоплазме 2) в ядре 3) в митохондриях
4) на мембранах шероховатой эндоплазматической сети
14. Одна аминокислота кодируется:
1) четырьмя нуклеотидами 2) двумя нуклеотидами
3) одним нуклеотидом 4) тремя нуклеотидами
15. Триплету нуклеотидов АТЦ в молекуле ДНК будет соответствовать кодон молекулы и-РНК:
1) ТАГ 2) УАГ 3) УТЦ 4) ЦАУ
16. На мембранах гранулярной эндоплазматической сети происходит синтез: 1) АТФ; 2) углеводов; 3) липидов; 4) белков.
17. Из общего содержания РНК клетки на долю и-РНК приходится примерно: 1) 0, 5-1 %; 2) 10 %; 3) 50 %; 4) 90%.
18. Среди молекул РНК больше всего по количеству:
1) т-РНК; 3) р-РНК; 2) и-РНК; 4) всех видов РНК примерно поровну.
В 1. Выберите признаки, соответствующие особенностям белкового обмена в организме человека.
A) Расщепление молекулы белка до аминокислот происходит в клетках
Б) Расщепление молекулы белка до аминокислот происходит в пищеварительном тракте
B) Конечными продуктами распада являются углекислый газ, вода, мочевина и другие вещества
Г) Конечными продуктами распада являются глюкоза, жирные кислоты
Д) Суточная потребность составляет 100-150 г
Е) Суточная потребность в белках - 400-600 г
В 2. Определите последовательность реакций матричного синтеза белка
A) Объединение и-РНК с рибосомой
Б) Ферментативный разрыв водородных связей молекулы ДНК
B) Синтез и-РНК на участке одной из цепей ДНК
Г) Объединение т-РНК с рибосомой и узнавание своего кодов
Д) Присоединение аминокислоты к т-РНК
Е) Отделение белковой цепи от т-РНК
В 3. Соотнесите особенности процессов биосинтеза белка и фотосинтеза
Особенности процесса
1) Завершается образованием углеводов
2) Исходные вещества - аминокислоты
3) В основе лежат реакции матричного синтеза
4) Исходные вещества - углекислый газ и вода
5) АТФ синтезируется в ходе процесса
6) АТФ используется для протекания процесса
Процессы
А) Биосинтез белка
Б) Фотосинтез
В 4. Установите соответствие между биологическим процессом и его свойствами:
СВОЙСТВОВ 4. Установите соответствие между биологическим процессом и его свойствами:
СВОЙСТВО
А) представляет собой синтез РНК на матрице ДНК
Б) происходит в цитоплазме
В) удвоение молекулы ДНК
Г) происходит на рибосомах
Д) представляет собой синтез белка
БИОЛОГИЧЕСКИЙ ПРОЦЕСС
1) транскрипция
2) трансляция
3) репликация
В 5. Укажите последовательность явлений и процессов, происходят в процессе синтеза белка:
A) поступление молекулы иРНК из ядра в цитоплазму
Б) взаимодействие молекулы тРНК, несущей первую аминокислоту данного белка, с рибосомой в комплексе с иРНК
B) образование пептидной связи
Г) синтез молекулы иРНК на матрице ДНК
Д) терминация трансляции
Е) связывание молекулы иРНК с рибосомой
В 6. Постройте последовательность реакций трансляции, выписав цифры в нужном порядке.
A) Присоединение аминокислоты к тРНК
Б) Начало синтеза полипептидной цепи на рибосоме
B) Присоединение иРНК к рибосоме
Г) Окончание синтеза белка
Д) Удлинение полипептидной цепи
Е) Соединение кодона с антикодоном
В 7. Установите последовательность этапов синтеза белка:
A) Попадание фрагмента и-РНК в акцепторный участок функционального центра рибосомы (ФЦР) ;
Б) Присоединение т-РНК с аминокислотой к соответствующему кодону и-РНК в акцепторном участке ФЦР;
B) Перемещение т-РНК с растущим белком в донорный участок ФЦР;
Г) Транскрипция;
Д) Удлинение полипептидной цепи на одну аминокислоту;
Е) Присоединение аминокислот к соответствующим т-РНК.
Доказано существование 4 уровней структурной организации белковой молекулы.
Первичная структура белка – последовательность расположения аминокислотных остатков в полипептидной цепи. В белках отдельные аминокислоты связаны друг с другом пептидными связями , возникающими при взаимодействии a-карбоксильных и a-аминогрупп аминокислот.
К настоящему времени расшифрована первичная структура десятков тысяч разных белков. Для определения первичной структуры белка методами гидролиза выясняют аминокислотный состав. Затем определяют химическую природу концевых аминокислот. Следующий этап - определение последовательности аминокислот в полипептидной цепи. Для этого используют избирательный частичный (химический и ферментативный) гидролиз. Возможно применение рентгеноструктурного анализа, а также данных о комплементарной нуклеотидной последовательности ДНК.
Вторичная структура белка – конфигурация полипептидной цепи, т.е. способ упаковки полипептидной цепи в определенную конформацию. Процесс этот протекает не хаотично, а в соответствии с программой, заложенной в первичной структуре.
Стабильность вторичной структуры обеспечивается в основном водородными связями, однако определенный вклад вносят ковалентные связи – пептидные и дисульфидные.
Наиболее вероятным типом строения глобулярных белков считают a-спираль . Закручивание полипептидной цепи происходит по часовой стрелке. Для каждого белка характерна определенная степень спирализации. Если цепи гемоглобина спирализованы на 75%, то пепсина-всего на 30%.
Тип конфигурации полипептидных цепей, обнаруженных в белках волос, шелка, мышц, получил название b-структуры . Сегменты пептидной цепи располагаются в один слой, образуя фигуру, подобную листу, сложенному в гармошку. Слой может быть образован двумя или большим количеством пептидных цепей.
В природе существуют белки, строение которых не соответствует ни β-, ни a-структуре, например, коллаген - фибриллярный белок, составляющий основную массу соединительной ткани в организме человека и животных.
Третичная структура белка – пространственная ориентация полипептидной спирали или способ укладки полипептидной цепи в определенном объеме. Первый белок, третичная структура которого была выяснена рентгеноструктурным анализом - миоглобин кашалота (рис. 2).
В стабилизации пространственной структуры белков, помимо ковалентных связей, основную роль играют нековалентные связи (водородные, электростатические взаимодействия заряженных групп, межмолекулярные ван-дер-ваальсовы силы, гидрофобные взаимодействия и т.д.).
По современным представлениям, третичная структура белка после завершения его синтеза формируется самопроизвольно. Основной движущей силой является взаимодействие радикалов аминокислот с молекулами воды. При этом неполярные гидрофобные радикалы аминокислот погружаются внутрь белковой молекулы, а полярные радикалы ориентируются в сторону воды. Процесс формирование нативной пространственной структуры полипептидной цепи называют фолдингом . Из клеток выделены белки, названные шаперонами. Они участвуют в фолдинге. Описан ряд наследственных заболеваний человека, развитие которых связывают с нарушением вследствие мутаций процесса фолдинга (пигментозы, фиброзы и др.).
Методами рентгеноструктурного анализа доказано существование уровней структурной организации белковой молекулы, промежуточных между вторичной и третичной структурами. Домен - это компактная глобулярная структурная единица внутри полипептидной цепи (рис. 3). Открыто много белков (например, иммуноглобулины), состоящих из разных по структуре и функциям доменов, кодируемых разными генами.
Все биологические свойства белков связаны с сохранностью их третичной структуры, которую называют нативной . Белковая глобула не является абсолютно жесткой структурой: возможны обратимые перемещения частей пептидной цепи. Эти изменения не нарушают общей конформации молекулы. На конформацию молекулы белка оказывают влияние рН среды, ионная сила раствора, взаимодействие с другими веществами. Любые воздействия, приводящие к нарушению нативной конформации молекулы, сопровождаются частичной или полной потерей белком его биологических свойств.
Четвертичная структура белка - способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой или разной первичной, вторичной или третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярного образования.
Белковую молекулу, состоящую из нескольких полипептидных цепей, называют олигомером , а каждую входящую в него цепь - протомером . Олигомерные белки чаще построены из четного числа протомеров, например, молекула гемоглобина состоит из двух a- и двух b-полипептидных цепей (рис. 4).
Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуноглобулины. Субъединичное строение свойственно многим ферментам.
Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. Биологическую активность белок приобретает только при объединении входящих в его состав протомеров. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной.
Некоторые исследователи признают существование пятого уровня структурной организации белков. Это метаболоны - полифункциональные макромолекулярные комплексы разных ферментов, катализирующих весь путь превращений субстрата (синтетазы высших жирных кислот, пируватдегидрогеназный комплекс, дыхательная цепь).
Биологическая химия Лелевич Владимир Валерьянович
Уровни структурной организации белков
Первичная структура – строго определенная линейная последовательность аминокислот в полипептидной цепочке.
Стратегические принципы изучения первичной структуры белка претерпевали значительные изменения по мере развития и усовершенствования применяемых методов. Следует отметить три основных этапа в их развитии. Первый этап начинается с классической работы Ф. Сенгера (1953) по установлению аминокислотной последовательности инсулина, второй – с широкого введения в структурный анализ белка автоматического секвенатора (начало 70-х годов 20 века), третий – с разработки скоростных методов анализа нуклеотидной последовательности ДНК (начало 80-х годов 20 века).
Первичная структура белка определяется:
1. Природой входящих в молекулу аминокислот.
2. Относительным количеством каждой аминокислоты.
3. Строго определенной последовательностью аминокислот в полипептидной цепи.
Предварительные исследования перед определением первичной структуры белка
1. Очистка белка
2. Определение молекулярной массы.
3. Определение типа и числа простетических групп (если белок конъюгированный).
4. Определение наличия внутри- или межмолекулярных дисульфидных связей. Обычно одновременно определяют наличие в нативном белке сульфгидрильных групп.
5. Предварительная обработка белков, обладающих 4-й структурой, с целью диссоциации субъединиц, их выделения и последующего изучения.
Стадии определения первичной структуры белков и полипептидов
1. Определение аминокислотного состава (гидролиз, аминокислотный анализатор).
2. Идентификация N- и С-концевых аминокислот.
3. Расщепление полипептидной цепи на фрагменты (трипсин, химотрипсин, бромциан, гидроксиламин и др.).
4. Определение аминокислотной последовательности пептидных фрагментов (секвенатор).
5. Расщепление исходной полипептидной цепи другими способами и установление их аминокислотной последовательности.
6. Установление порядка расположения пептидных фрагментов по перекрывающимся участкам (получение пептидных карт).
Методы определения N-концевых аминокислот
1. Метод Сенгера.
2. Метод Эдмана (реализован в секвенаторе).
3. Реакция с дансилхлоридом.
4. Метод с применением аминопептидазы.
Методы определения С-концевых аминокислот
1. Метод Акабори.
2. Метод с применением карбоксипептидазы.
3. Метод с применением боргидрида натрия.
Общие закономерности, касающиеся аминокислотной последовательности белков
1. Не существует одной уникальной последовательности или группы частичных последовательностей, общих для всех белков.
2. Белки, выполняющие разные функции, имеют разные последовательности.
3. Белки со схожими функциями имеют похожие последовательности, однако совпадение последовательности проявляется обычно лишь в малой степени.
4. Одинаковые белки, выполняющие одинаковые функции, но выделенные из разных организмов, обычно имеют значительное сходство в последовательности.
5. Одинаковые белки, выполняющие одинаковые функции и выделенные из организмов одного вида, почти всегда обладают совершенно одинаковой последовательностью.
Высшие уровни структуры белков, их биологическая активность тесно связаны и фактически определяются аминокислотной последовательностью. То есть, первичная структура генетически детерминирована и определяет индивидуальные свойства белков, их видовую специфичность, на ее основе формируются все последующие структуры.
Вторичная структура белка – конфигурация полипептидной цепи, образующаяся в результате взаимодействий между её функциональными группами.
Разновидности вторичной структуры:
1. ?-спираль.
2. Складчатый лист (?-структура).
3. Статистический клубок.
Первые две разновидности представляют собой упорядоченное расположение, третья – неупорядоченное.
Супервторичная структура белков.
Сравнение конформаций разных по структуре и функциям белков выявило наличие у них похожих сочетаний элементов вторичной структуры. Такой специфический порядок формирования вторичных структур называют супервторичной структурой. Супервторичная структура формируется за счет межрадикальных взаимодействий.
Разновидности супервторичной структуры белков:
1. Супервторичная структура типа?-бочонка. Она действительно напоминает бочонок, где каждая?-структура расположена внутри и связана?-спиральным участком цепи, находящимся на поверхности. Характерна для некоторых ферментов – триозофосфатизомеразы, пируваткиназы.
2. Структурный мотив «?-спираль – поворот – ?-спираль». Обнаружен во многих ДНК-связывающих белках.
3. Супервторичная структура в виде «цинкового пальца». Характерна также для ДНК-связывающих белков. «Цинковый палец» – фрагмент белка, содержащий около 20 аминокислот, в котором атом цинка связан с радикалами четырех аминокислот: обычно с двумя остатками цистеина и двумя – гистидина.
4. Супервторичная структура в виде «лейциновой застежки-молнии». Объединение протомеров или отдельных белков в комплексы иногда осуществляется с помощью структурных мотивов, называемых «лейциновая застежка-молния». Примером такого соединения белков могут служить гистоны. Это ядерные белки, в состав которых входит большое количество положительно заряженных аминокислот – аргинина и лизина. Молекулы гистонов объединяются в комплексы с помощью «лейциновых застежек», несмотря на то, что все мономеры имеют сильный положительный заряд.
По наличию?-спиралей и?-структур глобулярные белки можно разделить на 4 категории:
Третичная структура белка – пространственная ориентация полипептидной цепи или способ ее укладки в определенном объеме.
В зависимости от формы третичной структуры различают глобулярные и фибриллярные белки. В глобулярных белках чаще преобладает?-спираль, фибриллярные белки образуются на основе?-структуры.
В стабилизации третичной структуры глобулярного белка могут принимать участие:
1. водородные связи спиральной структуры;
2. водородные связи?-структуры;
3. водородные связи между радикалами боковых цепей;
4. гидрофобные взаимодействия между неполярными группами;
5. электростатические взаимодействия между противоположно заряженными группами;
6. дисульфидные связи;
7. координационные связи ионов металлов.
Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой (или различной) первичной, вторичной или третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярного образования.
Четвертичная структура характерна для белков, состоящих из нескольких субъединиц. Взаимодействие между комплементарными участками субъединиц в четвертичной структуре осуществляется с помощью водородных и ионных связей, ван-дер-ваальсовых сил, гидрофобных взаимодействий. Реже возникают ковалентные связи.
Преимущества субъединичного построения белков по сравнению с одной длинной полипептидной цепью.
Во-первых, наличие субъединичной структуры позволяет «экономить» генетический материал. Для олигомерных белков, состоящих из идентичных субъединиц, резко уменьшается размер структурного гена и, соответственно, длина матричной РНК.
Во-вторых, при сравнительно небольшой величине цепей уменьшается влияние случайных ошибок, которые могут возникнуть в процессе биосинтеза белковых молекул. Кроме того, возможна дополнительная выбраковка «неправильных», ошибочных полипептидов в процессе ассоциации субъединиц в единый комплекс.
В-третьих, наличие субъединичной структуры у многих белков позволяет клетке легко регулировать их активность путем смещения равновесия «ассоциация-диссоциация» в ту или иную сторону.
Наконец, субъединичная структура облегчает и ускоряет процесс молекулярной эволюции. Мутации, приводящие лишь к небольшим конформационным изменениям на уровне третичной структуры за счет многократного усиления этих изменений при переходе к четвертичной структуре, могут способствовать появлению у белка новых свойств.
Из книги Биология [Полный справочник для подготовки к ЕГЭ] автора Лернер Георгий Исаакович Из книги Недостающее звено автора Иди МейтлендГенеалогическое древо (свидетельство белков) Генеалогическое древо (свидетельство белков)Различия в белках двух видов отражают эволюционные изменения этих видов после их отделения от общего предка. Анализ показывает, что между альбуминами кровяных сывороток шимпанзе
Из книги Беседы о жизни автора Галактионов Станислав ГеннадиевичГлава 2. Молекулярная архитектура белков Не будем скрывать: покончив с первой главой, авторы (а возможно, и читатель) испытали некоторое облегчение. В конце концов цель ее заключалась лишь в том, чтобы дать читателю сведения, необходимые для понимания последующих глав,
Из книги Эволюция [Классические идеи в свете новых открытий] автораВселенная древних белков продолжает расширяться В 2010 году журнал Nature опубликовал интересную статью об эволюционном движении белков по ландшафтам приспособленности (Povolotskaya, Kondrashov, 2010). Авторы работы решили сравнить аминокислотные последовательности 572 древних белков,
Из книги Гены и развитие организма автора Нейфах Александр Александрович4. Варианты структурной гипотезы Итак, несколько экспериментальных данных говорят о возможности таких структурных изменений, которые сохраняются при митозе и при репликации, могут передаваться в ряду клеточных поколений и обеспечивают эпигенетическую
Из книги Эволюция человека. Книга 1. Обезьяны, кости и гены автора Марков Александр ВладимировичИзменения белков Те участки генома, которые кодируют белки, изменились на удивление мало. Различия в аминокислотных последовательностях белков у человека и шимпанзе составляют значительно менее 1 %, да и из этих немногочисленных различий большая часть либо не имеет
Из книги Биология. Общая биология. 10 класс. Базовый уровень автора Сивоглазов Владислав Иванович3. Уровни организации живой материи. Методы биологии Вспомните!Какие уровни организации живой материи вам известны?Какие вы знаете методы научных исследований?Уровни организации живой материи. Окружающий нас мир живых существ – это совокупность биологических систем
Из книги Антропология и концепции биологии автора Курчанов Николай АнатольевичСтруктурно-функциональные уровни организации жизни В биологии различают несколько структурно-функциональных уровней организации живой материи.Молекулярный уровень. Характеризуется биохимическими веществами, составляющими живой организм.Клеточный уровень.
Из книги Биологическая химия автора Лелевич Владимир ВалерьяновичГлава 2. Строение и функции белков Белки – высокомолекулярные азотсодержащие органические соединения, состоящие из аминокислот, соединенных в полипептидные цепи с помощью пептидных связей, и имеющие сложную структурную организацию.История изучения белковВ 1728 г.
Из книги автораФункционирование белков Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей его от всех остальных белков. Набор индивидуальных белков выполняет в клетке множество разнообразных и сложных
Из книги автораПосттрансляционные изменения белков Многие белки синтезируются в неактивном виде (предшественники) и после схождения с рибосом подвергаются постсинтетическим структурным модификациям. Эти конформационные и структурные изменения полипептидных цепей получили
Из книги автораУровни изучения обмена веществ Уровни изучения обмена веществ:1. Целый организм.2. Изолированные органы (перфузируемые).3. Срезы тканей.4. Культуры клеток.5. Гомогенаты тканей.6. Изолированные клеточные органеллы.7. Молекулярный уровень (очищенные ферменты, рецепторы и
Из книги автораПереваривание белков в желудочно-кишечном тракте Переваривание белков начинается в желудке под действием ферментов желудочного сока. За сутки его выделяется до 2,5 литров и он отличается от других пищеварительных соков сильно кислой реакцией, благодаря присутствию
Из книги автораРасщепление белков в тканях Осуществляется с помощью протеолитических лизосомальных ферментов катепсинов. По строению активного центра выделяют цистеиновые, сериновые, карбоксильные и металлопротеиновые катепсины. Роль катепсинов:1. создание биологически активных
Из книги автораРоль печени в обмене аминокислот и белков Печень играет центральную роль в обмене белков и других азотсодержащих соединений. Она выполняет следующие функции:1. синтез специфических белков плазмы: - в печени синтезируется: 100 % альбуминов, 75 – 90 % ?-глобулинов, 50 %
Из книги автораХарактеристика белков сыворотки крови Белки системы комплемента – к этой системе относятся 20 белков, циркулирующих в крови в форме неактивных предшественников. Их активация происходит под действием специфических веществ, обладающих протеолитической активностью.
Белки — высокомолекулярные органические соединения, состоящие из остатков α-аминокислот.
В состав белков входят углерод, водород, азот, кислород, сера. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь.
Белки обладают большой молекулярной массой: яичный альбумин — 36 000, гемоглобин — 152 000, миозин — 500 000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78.
Аминокислотный состав белков
Белки — непериодические полимеры, мономерами которых являются α-аминокислоты . Обычно в качестве мономеров белков называют 20 видов α-аминокислот, хотя в клетках и тканях их обнаружено свыше 170.
В зависимости от того, могут ли аминокислоты синтезироваться в организме человека и других животных, различают: заменимые аминокислоты — могут синтезироваться; незаменимые аминокислоты — не могут синтезироваться. Незаменимые аминокислоты должны поступать в организм вместе с пищей. Растения синтезируют все виды аминокислот.
В зависимости от аминокислотного состава, белки бывают: полноценными — содержат весь набор аминокислот; неполноценными — какие-то аминокислоты в их составе отсутствуют. Если белки состоят только из аминокислот, их называют простыми . Если белки содержат помимо аминокислот еще и неаминокислотный компонент (простетическую группу), их называют сложными . Простетическая группа может быть представлена металлами (металлопротеины), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины).
Все аминокислоты содержат : 1) карбоксильную группу (-СООН), 2) аминогруппу (-NH 2), 3) радикал или R-группу (остальная часть молекулы). Строение радикала у разных видов аминокислот — различное. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты , имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты , имеющие более одной аминогруппы; кислые аминокислоты , имеющие более одной карбоксильной группы.
Аминокислоты являются амфотерными соединениями , так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах.
Пептидная связь
Пептиды — органические вещества, состоящие из остатков аминокислот, соединенных пептидной связью.
Образование пептидов происходит в результате реакции конденсации аминокислот. При взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой между ними возникает ковалентная азот-углеродная связь, которую и называют пептидной . В зависимости от количества аминокислотных остатков, входящих в состав пептида, различают дипептиды, трипептиды, тетрапептиды и т.д. Образование пептидной связи может повторяться многократно. Это приводит к образованию полипептидов . На одном конце пептида находится свободная аминогруппа (его называют N-концом), а на другом — свободная карбоксильная группа (его называют С-концом).

Пространственная организация белковых молекул
Выполнение белками определенных специфических функций зависит от пространственной конфигурации их молекул, кроме того, клетке энергетически невыгодно держать белки в развернутой форме, в виде цепочки, поэтому полипептидные цепи подвергаются укладке, приобретая определенную трехмерную структуру, или конформацию. Выделяют 4 уровня пространственной организации белков .
Первичная структура белка — последовательность расположения аминокислотных остатков в полипептидной цепи, составляющей молекулу белка. Связь между аминокислотами — пептидная.

Если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 10 20 . Имея 20 аминокислот, можно составить из них еще большее количество разнообразных комбинаций. В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов.
Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
Вторичная структура — упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Практически все СО- и NН-группы принимают участие в образовании водородных связей. Они слабее пептидных, но, повторяясь многократно, придают данной конфигурации устойчивость и жесткость. На уровне вторичной структуры существуют белки: фиброин (шелк, паутина), кератин (волосы, ногти), коллаген (сухожилия).



Третичная структура — укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков. Основную роль в образовании третичной структуры играют гидрофильно-гидрофобные взаимодействия. В водных растворах гидрофобные радикалы стремятся спрятаться от воды, группируясь внутри глобулы, в то время как гидрофильные радикалы в результате гидратации (взаимодействия с диполями воды) стремятся оказаться на поверхности молекулы. У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями, возникающими между атомами серы двух остатков цистеина. На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны.

Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Иногда при образовании четвертичной структуры между субъединицами возникают дисульфидные связи. Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин . Он образован двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо.
Если по каким-либо причинам пространственная конформация белков отклоняется от нормальной, белок не может выполнять свои функции. Например, причиной «коровьего бешенства» (губкообразной энцефалопатии) является аномальная конформация прионов — поверхностных белков нервных клеток.
Свойства белков
Аминокислотный состав, структура белковой молекулы определяют его свойства . Белки сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот: чем больше кислых аминокислот в белке, тем ярче выражены его кислотные свойства. Способность отдавать и присоединять Н + определяют буферные свойства белков ; один из самых мощных буферов — гемоглобин в эритроцитах, поддерживающий рН крови на постоянном уровне. Есть белки растворимые (фибриноген), есть нерастворимые, выполняющие механические функции (фиброин, кератин, коллаген). Есть белки активные в химическом отношении (ферменты), есть химически неактивные, устойчивые к воздействию различных условий внешней среды и крайне неустойчивые.
Внешние факторы (нагревание, ультрафиолетовое излучение, тяжелые металлы и их соли, изменения рН, радиация, обезвоживание)
могут вызывать нарушение структурной организации молекулы белка. Процесс утраты трехмерной конформации, присущей данной молекуле белка, называют денатурацией . Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные. Поэтому сначала утрачивается четвертичная, затем третичная и вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой , в этом случае происходит самовосстановление свойственной белку конформации. Такой денатурации подвергаются, например, рецепторные белки мембраны. Процесс восстановления структуры белка после денатурации называется ренатурацией . Если восстановление пространственной конфигурации белка невозможно, то денатурация называется необратимой .
Функции белков
| Функция | Примеры и пояснения |
|---|---|
| Строительная | Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
| Транспортная | Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
| Регуляторная | Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
| Защитная | В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки — антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений. |
| Двигательная | Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных. |
| Сигнальная | В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
| Запасающая | В организме животных белки, как правило, не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется, образуя комплекс с белком ферритином. |
| Энергетическая | При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
| Каталитическая | Одна из важнейших функций белков. Обеспечивается белками — ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Например, рибулезобифосфаткарбоксилаза катализирует фиксацию СО 2 при фотосинтезе. |
Ферменты
Ферменты , или энзимы , — особый класс белков, являющихся биологическими катализаторами. Благодаря ферментам биохимические реакции протекают с огромной скоростью. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов. Вещество, на которое оказывает свое действие фермент, называют субстратом .
Ферменты — глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные. Простые ферменты являются простыми белками, т.е. состоят только из аминокислот. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор . У некоторых ферментов в качестве кофакторов выступают витамины. В молекуле фермента выделяют особую часть, называемую активным центром. Активный центр — небольшой участок фермента (от трех до двенадцати аминокислотных остатков), где и происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции. Некоторые ферменты имеют (кроме активного) аллостерические центры — участки, к которым присоединяются регуляторы скорости работы фермента (аллостерические ферменты ).

Для реакций ферментативного катализа характерны: 1) высокая эффективность, 2) строгая избирательность и направленность действия, 3) субстратная специфичность, 4) тонкая и точная регуляция. Субстратную и реакционную специфичность реакций ферментативного катализа объясняют гипотезы Э. Фишера (1890 г.) и Д. Кошланда (1959 г.).
Э. Фишер (гипотеза «ключ-замок») предположил, что пространственные конфигурации активного центра фермента и субстрата должны точно соответствовать друг другу. Субстрат сравнивается с «ключом», фермент — с «замком».
Д. Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Эту гипотезу еще называют гипотезой индуцированного соответствия .
Скорость ферментативных реакций зависит от: 1) температуры, 2) концентрации фермента, 3) концентрации субстрата, 4) рН. Следует подчеркнуть, что поскольку ферменты являются белками, то их активность наиболее высока при физиологически нормальных условиях.
Большинство ферментов может работать только при температуре от 0 до 40 °С. В этих пределах скорость реакции повышается примерно в 2 раза при повышении температуры на каждые 10 °С. При температуре выше 40 °С белок подвергается денатурации и активность фермента падает. При температуре, близкой к точке замерзания, ферменты инактивируются.
При увеличении количества субстрата скорость ферментативной реакции растет до тех пор, пока количество молекул субстрата не станет равным количеству молекул фермента. При дальнейшем увеличении количества субстрата скорость увеличиваться не будет, так как происходит насыщение активных центров фермента. Увеличение концентрации фермента приводит к усилению каталитической активности, так как в единицу времени преобразованиям подвергается большее количество молекул субстрата.

Для каждого фермента существует оптимальное значение рН, при котором он проявляет максимальную активность (пепсин — 2,0, амилаза слюны — 6,8, липаза поджелудочной железы — 9,0). При более высоких или низких значениях рН активность фермента снижается. При резких сдвигах рН фермент денатурирует.
Скорость работы аллостерических ферментов регулируется веществами, присоединяющимися к аллостерическим центрам. Если эти вещества ускоряют реакцию, они называются активаторами , если тормозят — ингибиторами .
Классификация ферментов
По типу катализируемых химических превращений ферменты разделены на 6 классов:
- оксиредуктазы (перенос атомов водорода, кислорода или электронов от одного вещества к другому — дегидрогеназа),
- трансферазы (перенос метильной, ацильной, фосфатной или аминогруппы от одного вещества к другому — трансаминаза),
- гидролазы (реакции гидролиза, при которых из субстрата образуются два продукта — амилаза, липаза),
- лиазы (негидролитическое присоединение к субстрату или отщепление от него группы атомов, при этом могут разрываться связи С-С, С-N, С-О, С-S — декарбоксилаза),
- изомеразы (внутримолекулярная перестройка — изомераза),
- лигазы (соединение двух молекул в результате образования связей С-С, С-N, С-О, С-S — синтетаза).
Классы в свою очередь подразделены на подклассы и подподклассы. В действующей международной классификации каждый фермент имеет определенный шифр, состоящий из четырех чисел, разделенных точками. Первое число — класс, второе — подкласс, третье — подподкласс, четвертое — порядковый номер фермента в данном подподклассе, например, шифр аргиназы — 3.5.3.1.
Перейти к лекции №2 «Строение и функции углеводов и липидов»
Перейти к лекции №4 «Строение и функции нуклеиновых кислот АТФ»




